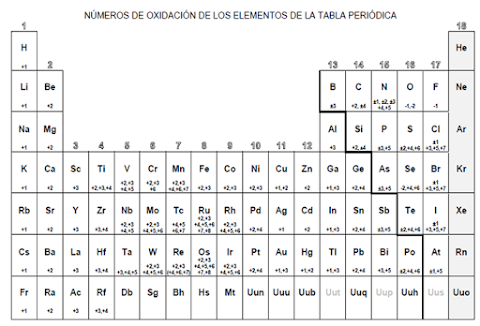
de un átomo de un compuesto, indica el numero de electrones que el átomo habría perdido o ganado si el compuesto fuera completamente iónico.
Debemos distinguir entre:
- Carga real: cuando forman iones mono atómicos
- Carga ficticia: Cuando comparten electrones, enlace covalente.
2. Valencia:
Es es número de electrones perdidos (valencia positiva) o ganados (valencia negativa) o compartidos al combinarse con otro
La electrovalencia es aquella en la que se pierden o ganan electrones.
La covalencia es en la que se comparten.
3. Elementos:
Los elementos químicos pueden dividirse en:
- Moleculares: Formados por moléculas de 10 o más átomos iguales. Se separan en monoatómicas (gases), diatómicas (gases excpeto el Br2 y el I2) y los sólidos (P4 y S8)
- Atómicos: Formados por una estructura gigante de átomos iguales. Son sólidos y solo 3: B, C y Si.
- Metálicos: Formados por cationes y una nube de electrones. Son sólidos, excepto el mercurio.
4. Compuestos:
- Moleculares: Binarios: no metal + no metal. Ternarios: Oxoácidos (HXO).
- Iónicos: Binarios: metal + no metal (hidruros, óxidos y sales). Ternarios: compuestos de amonio, Hidróxidos y Oxosales.
- Atómicos: Fromados por una estructura gigante de átomos. Son sólidos, Ej: SiO2, BN, SiC.
No hay comentarios:
Publicar un comentario