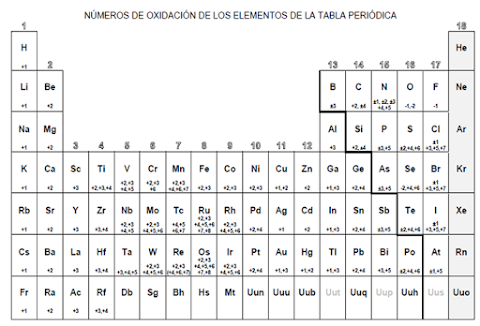
1. Número de oxidación:
de un átomo de un compuesto, indica el numero de electrones que el átomo habría perdido o ganado si el compuesto fuera completamente iónico.
Debemos distinguir entre:
- Carga real: cuando forman iones mono atómicos
- Carga ficticia: Cuando comparten electrones, enlace covalente.
2. Valencia:
Es es número de electrones perdidos (valencia positiva) o ganados (valencia negativa) o compartidos al combinarse con otro
La electrovalencia es aquella en la que se pierden o ganan electrones.
La covalencia es en la que se comparten.
3. Elementos:
Los elementos químicos pueden dividirse en:
- Moleculares: Formados por moléculas de 10 o más átomos iguales. Se separan en monoatómicas (gases), diatómicas (gases excpeto el Br2 y el I2) y los sólidos (P4 y S8)
- Atómicos: Formados por una estructura gigante de átomos iguales. Son sólidos y solo 3: B, C y Si.
- Metálicos: Formados por cationes y una nube de electrones. Son sólidos, excepto el mercurio.
- Moleculares: Binarios: no metal + no metal. Ternarios: Oxoácidos (HXO).
- Iónicos: Binarios: metal + no metal (hidruros, óxidos y sales). Ternarios: compuestos de amonio, Hidróxidos y Oxosales.
- Atómicos: Fromados por una estructura gigante de átomos. Son sólidos, Ej: SiO2, BN, SiC.
Leyes de la Química
1. Leyes Ponderales:
- Conservación de la masa: la masa total de las sustancias que intervienen en una reacción química permanece invariable, por tanto la masa total de las sustancias que reaccionan es igual a la masa de las sustancias que se originan.
- Proporciones definidas: Cuando dos elementos se combinan para originar un compuesto determinado, lo hacen siempre e una relación en masa constante.
- Proporciones múltiples: cuando se combinan dos elementos para formar más de un compuesto, una masa constante de uno de ellos se combina con masas variables del otro. Estas masas variables guardan entre sí una relación sencilla de números enteros.
2. Leyes Volumétricas:
- Volúmenes de combinación: en las reacciones entre gases, los volúmenes entre reactivos y de los productos están en una relación constante de números enteros sencillos.
- Ley de Avogadro: volúmenes iguales de distintos gases, sometidas a la misma presión y temperatura, contienen siempre el mismo número de moléculas.
3. Leyes de los Gases:
- Ley de Charles: a presión constante, el volumen de una masa de gas es estrictamente proporcional a su temperatura absoluta.
- Ley de Gay-Lussac: a volumen constante, la presión de una masa de gas es directamente proporcional a su temperatura absoluta.
- Ley de Boyle: a temperatura constante, el volumen de una masa de gas es inversamente proporcional a la presión.
4. Ley de Henry:
La solubilidad de un fas en un líquido a temperatura constante es directamente proporcional a la presión parcial del gas sobre la disolución.
Reacciones Químicas
Hay 4 tipos de reacciones químicas:
- Combustión: reacción química entre un combustible y un comburente que desprende luz y calor.

- Reacciones Ácido-Base: son aquellas en las que ocurre una transferencia de protones. La base puede ganas H+ y el ácido puede perder H+ para cederlos a una base. Las bases son el NH3 y los hidróxidos.
Los ácidos son los oxoácidos, hidrácidos y los ácidos orgánicos.
- Redox: son las de transferencia de electrones. La sustancia reductora cede electrones y se oxida (aumenta su número de ox). La sustancia oxidante capta electrones y se reduce (reduce su número de ox).

- Precipitación: mezclas de sustancias iónicas en disolución acuosa. Se produce una recombinación de átomos.
Ejercicios de Química
Estos son ejercicios típicos de química sacados de examanes. Vienen las soluciones en rojo.
Dibujar Compuestos:
Aquí les dejo unos ejemplos sobre como dibujar la estructura de Lewis de algunos compuestos químicos.
Para realizar una de estas estructuras hay que seguir los siguientes pasos:
- Escribir el compuesto y comprobar los números de oxidación.
- Escribir la configuración electrónica de los elementos que forman el compuesto.
- Ver si algún elemento promociona electrones.
- Dibujar la estructura básica.
- Dibujar la estructura del compuesto teniendo en cuenta los ángulos que se forman.

No hay comentarios:
Publicar un comentario